Kategóriák
- Vizsgálati kisokos (5)
- Egyéb kategória (17)
- Hírek (110)
- Betegségek (54)
C9orf72 génmutáció specifikus terápiás fejlesztések ALS-ban
Az amiotrófiás laterálszklerózis, röviden ALS egy izomsorvadással járó neurodegeneratív megbetegedés. Ismert, hogy az ALS esetek mintegy 10 százaléka mutat családi halmozódást, az esetek további 90 százaléka sporadikus eredetű.
2011-ben két független kutatócsoport azonosította a C9orf72 génben található, hat nukleotid egységből álló ismétlődés felszaporodást, ami az európai származású betegek körében a leggyakoribb genetikai eltérés az ALS hátterében. A sporadikus kóreredetű betegek 7 %-ában, a családi halmozódás mutató esetek akár 40%-ában is azonosítható ez a genetikai eltérés. Egészségesekben az ismétlődések számba nem haladja meg a 30-at, míg ALS betegek esetében akár 1000 ismétlődés is detektálható.
Több elmélet is magyarázni próbálja azt, hogy milyen módon vezet a betegség kialakulásához a kórosan hosszú ismétlődő génszakasz. Egyes meglátások szerint az ismétlődő szakasz abnormális hossza miatt a génről leíródó fehérje nem tudja ellátni a feladatát, ezáltal a mutáció funkcióvesztő módon befolyásolja a fehérje működését. Más elméletek szerint a hosszú, egymással komplementer szekvenciájú génszakaszról olyan fehérje termék íródik le, ami önmagával összegabalyodik és ez a gombolyagos forma nehezebbé teszi a fehérje lebontását. Ezen elképzelések szerint a mutáció következtében a fehérje egy eddig meg nem lévő, „plusz” tulajdonságot, funkciót nyer, tehát ezt a mutáció típust funkció nyeréses variánsnak hívjuk. A valóságban valószínűleg a funkcióvesztéses és a funkciónyeréses mechanizmus egymás mellett megfér, vélhetően mindkét mechanizmus hozzájárul a mutáció károsító szerepének kialakításához.
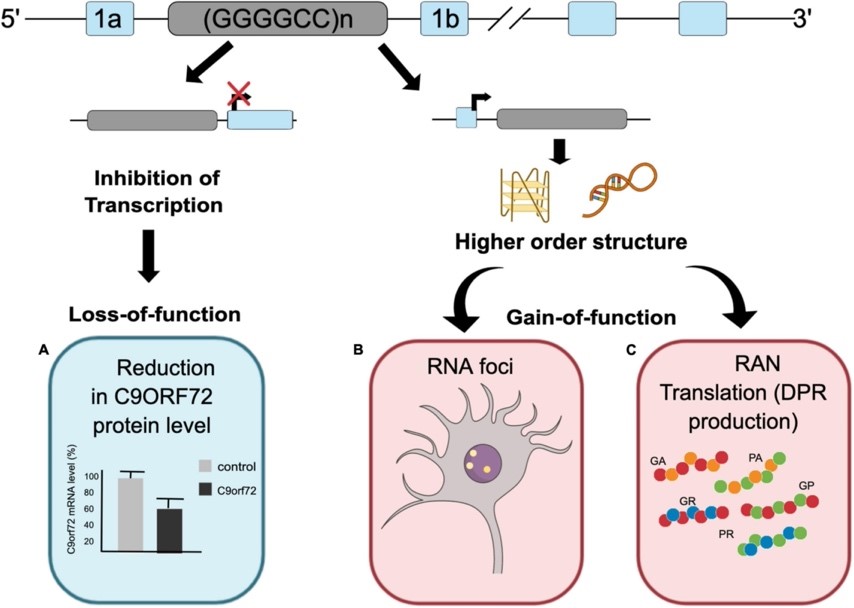
https://www.frontiersin.org/journals/cellular-neuroscience/articles/10.3389/fncel.2021.637548/full
A C9orf72 gén kóros hosszúságú ismétlődő szakaszait mind ALS, mind frontotemporális demencia hátterében azonosították. A C9orf72 mutációt hordozó ALS betegekre jellemző a viszonylag gyors betegséglefolyás, az alacsony betegségkezdetkori életkor, a száj körüli-, illetve nyelést segítő izmok korai érintettsége. Ez a géneltérés testi kromoszómához kötött domináns öröklésmenetet mutat, tehát egy beteg 50% eséllyel örökítheti tovább a genetikai eltérést az utódgenerációra nemtől függetlenül. Jelenleg is számos genetikailag célzott terápiás próbálkozás van fejlesztés alatt a C9orf72 pozitív betegek számára.
A Biogen gyógyszercég által fejlesztett és támogatott antisense oligonukleotid alapú, BIIB078 nevű szert a Fázis1 vizsgálatok során jól tolerálhatónak minősítették, viszont nem lassította a betegség lefolyását, így a fejlesztését 2022-ben megszakították. A BIIB078 kódszámú molekula hatásmechanizmusa alapján még a fehérjeszint előtt, a nukleotidok szintjén megakadályozná, hogy a C9orf72 génről fehérjetermék képződjön. A klinikai gyógyszer vizsgálat során 106 beteg részesült ebben a kísérleti kezelésben. A betegek hat különböző dózisban, átlagosan fél évig kapták a kísérleti kezelést lumbális injekció formájában. Összességében a terápia jól tolerálható volt, a legtöbb mellékhatás a lumbális injekció beadásából származott, súlyos mellékhatást nem jelentettek a vizsgálat során. Sajnos a kísérleti gyógyszer nem lassította a betegség lefolyását a kontrollcsoporthoz képest, sem nem javult a betegek életminősége, így a gyógyszercég arra következtetésre jutott, hogy a fejlesztést leállítja.
A Transposon Therapeutics nevű gyógyszercég egy másik, TPN-101 névre hallgató, szájon át szedhető molekulát tesztel C9orf72 pozitív ALS betegek körében. Jelenleg a Fázis1-2a fejlesztési szakaszok adatai állnak rendelkezésre: összesen 42 beteg vett részt a kísérleti fázisban, a TPN-101-el kezelt csoportban lassabban előrehaladó csökkenést észleltek a légzésfunkciós értékeket tekintve. Mindeközben biokémiai szinten szignifikánsan csökkent az idegsejtek pusztulásának és az idegrendszeri gyulladások egyik markere.
A TPN-101 molekula egy transzpozon elem reverz transzkriptáz enzimének gátlója. De hogy miért is van ennek köze az állás kezeléséhez? A transzpozonok olyan genetikai elemek, amik az evolúció során épültek be az emberi genetikai állományba vélhetően vírusokból. Ezek a genetikai elemek a génkifejeződés szabályozása által szigorúan korlátozva vannak, nem tudnak fehérjét termelni. Bizonyos keretek között ezek a transzpozonok aktiválódni tudnak, és ilyenkor fehérje íródik le ezekről a DNS szakaszokról, úgy mintha egy vírusról termelődne fehérje. Ez egy immunreakciót indít be, ami gyulladáshoz vezet, akár a központi idegrendszerben is. A TPN-101 molekula ezt az immun aktivációt hivatott gátolni, és ezzel csökkenti az idegrendszeri gyulladást és az idegsejt pusztulást.
A kísérleti molekulát szedő csoport légzésfunkciós paraméterei fele olyan lassan csökkentek, mint a kontrollcsoporté. Miután 24 hét placebo után a kontrollcsoport betegei is átkerültek a kísérleti szert kapó betegek közé, az eredetileg kontrollcsoportba tartozó betegek légzésfunkciós értékeinek csökkenése szinte megállt, egy évvel a vizsgálat kezdetét követően a két csoport (48 hét TPN-101 vs. 24 hét placebo és 24 hét TPN-101) légzésfunkciós paraméterei szinte megegyeztek.
A kísérleti szer betegség lefolyást lassító hatása csupán a végéig gyógyszert kapó csoportban volt szignifikáns. A 48 hét végére a TPN-101 kezelésben részesülő betegek állapota az átlagnál 40%-kal lassabban romlott, míg a placebot kapó betegekhez viszonyítva az állapotuk 48 hét alatt fele olyan lassan romlott. A gyógyszercég a pozitív eredmények birtokában szeretné a molekulát Fázis3 vizsgálatokba tovább vinni.
Források:
- https://www.frontiersin.org/journals/cellular-neuroscience/articles/10.3389/fncel.2021.637548/full
- https://alsnewstoday.com/news/tpn-101-shows-long-term-benefits-c9orf72-related-als-trial/
- https://alsnewstoday.com/news/discontinued-therapy-biib078-not-effective-als-trial-data/
- https://clinicaltrials.gov/study/NCT04993755
Szerkesztette: dr. Nagy Zsófia Flóra
2024. augusztus 03.