Kategóriák
- Vizsgálati kisokos (5)
- Egyéb kategória (17)
- Hírek (110)
- Betegségek (54)
Leállították a célzott C9orf72 asszociált ALS elleni szer, a BIIB078 fejlesztését
A gyógyszer fejlesztését 2022-ben leállították a klinikai előny hiánya miatt, ugyanakkor a kutatók remélik, hogy az új adatok hozzájárulnak majd jobb ASO-terápiák kifejlesztéséhez.
Mik azok az ASO-k?
Az ASO-k (antisense oligonukleotid) rövid, mesterségesen előállított nukleinsav-szakaszok (általában 15-25 bázis hosszú DNS- vagy RNS-darab). Úgy tervezték meg biomérnökileg, hogy pontosan hozzákötődjön egy adott gén hírvivő RNS-éhez (mRNS), ezáltal gátolja a kóros fehérje termelődését, mert az mRNS-t lebontásra jelöli vagy megakadályozza annak átíródását fehérjére. Célzott, génszintű beavatkozási lehetőséget biztosít, amely közvetlenül a betegség gyökerét próbálja kezelni, viszont hátránya lehet, hogy nem mindig jut be elég hatékonyan a központi idegrendszerbe, és előfordulhat, hogy a betegség összetett kóros folyamatait nem tudja teljesen befolyásolni.
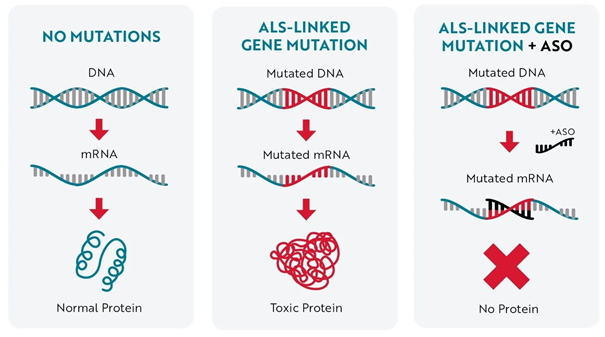
1 . ábra. A Qalsody (tofersen) hatásmechanizmusa. A bal oldali ábrán látható a normális élettani helyzet. A középső ábrán egy kezelésben nem részesülő, SOD1 mutációt hordozó beteg esete látható: A mutációt hordozó génről egy igen stabil, a lebontásnak ellenálló fehérjetermék képződik. A jobb oldali ábrán látható a Qalsody kezelés (az ábrán ASO-ként jelölve) hatása: még mielőtt fehérje képződne, a gyógyszer megakadályozza a fehérjetermék képződését, így nem keletkezik ez a lebontásnak ellenálló toxikus fehérje.
Ebbe az osztályba tartozik a már engedélyezett célzott ALS-terápia, a Qalsody (tofersen) is, valamint az SMA betegségmódosító terápiái közül a nusinersen (Spinraza) valamint számos kísérleti fázisban lévő készítmény.
Pontosabb elemzések a BIIB078 hatástalanságának okairól
Oldalunkon korábban is írtunk a BIIB078 fejlesztésének leállításáról. A vizsgálati fázisban lévő antiszensz oligonukleotid (ASO) terápia, a BIIB078, azért bukhatott meg az amiotrófiás laterálszklerózis (ALS) klinikai vizsgálataiban, mert nem fordította vissza az elvárt mértékben az agyban és a gerincvelőben zajló kulcsfontosságú kóros folyamatokat. A résztvevőktől származó testfolyadékok és szövetek elemzése kimutatta, hogy bár a BIIB078 eljutott a célzott szövetekhez, nem tudta teljesen megakadályozni a
toxikus fehérjék felhalmozódását és más, a betegség progressziójához hozzájáruló molekulák termelődését.
A Biogen és az Ionis közösen fejlesztette a BIIB078-at is, amely a C9orf72 hexanukleotid ismétlődései ellen volt hivatott hatni, hogy elnyomja a toxikus fehérjék termelődését.
Egy 1. fázisú klinikai vizsgálat (NCT03626012) és annak nyílt kiterjesztéses szakasza (NCT04288856) a gyógyszer biztonságosságát és tolerálhatóságát tesztelte C9orf72 hexanukleotid repeat expanzióhoz társult ALS-sal élő felnőtteknél. Az adatok szerint a BIIB078 csökkentette a toxikus fehérjeszinteket az agyat és gerincvelőt körülvevő agy-gerincvelői folyadékban (liqour), de a résztvevők egyik dózisnál sem mutattak klinikai javulást a placebóhoz képest. Bár a liqourból mérhető biomarkerek javulást mutattak, nem volt egyértelmű, hogy a szer valóban eljutott-e a központi idegrendszeri szövetekbe, és képes-e befolyásolni a betegség lefolyását.
Egy friss elemzésben a kutatók újra megvizsgálták a vizsgálatban részt vevő betegek liquor- és a halál után nyert agyszövetmintáit. A vizsgálatban 8 C9orf72 hexanukleotid repeat expanziót hordozó ALS beteg kapott BIIB078-at, míg 31 C9orf72-ALS beteg nem kapta a kísérleti szert, továbbá 32 egészséges kontroll vett részt a klinikai vizsgálatban. Az eredmények kimutatták, hogy ugyan a BIIB078 eljutott a központi idegrendszerbe, és széles körben eloszlott a betegség szempontjából kulcsfontosságú régiókban (gerincvelő, motoros kéreg), a fő kóroki tényezők – például a TDP-43 fehérje toxikus felhalmozódása és az
ismétlődő szekvenciából származó abnormális RNS-molekulák – továbbra is fennmaradtak. A biológiai válaszok széles skálán mozgó egyéni eltéréseket mutattak, és nem korreláltak megbízhatóan a betegség progressziójának klinikai mutatóival.
Ugyanakkor a kutatók szerint azonban a BIIB078 terápiás koncepciójának elvetése idő előtti lehet, még ha klinikailag sikertelennek is bizonyult. Ezek az új adatok viszont segíthetnek hatékonyabb ASO-k tervezésében.
A BIIB078 nem az egyetlen ASO-jelölt, amelyet a Biogen és az Ionis leállított: korábban a BIIB105-öt is fejlesztették, amely az ATXN2 gén ellen irányult, de szintén a klinikai hatásosság hiánya miatt állították le.
Irodalom:
https://alsnewstoday.com/news/failed-als-drug-biibo78-offer-clues-therapies-study-
finds/
McEachin, Zachary T et al. “Molecular impact of antisense oligonucleotide therapy in
C9orf72-associated ALS.” Cell, S0092-8674(25)00908-0. 26 Aug. 2025,
doi:10.1016/j.cell.2025.07.045 (https://www.cell.com/cell/fulltext/S0092-
8674(25)00908-0)
Készítette: dr. Nagy Zsófia Flóra
2025. október 24.